1) Généralité 2
Déf : La maladie de Parkinson (dites parfois « idiopathique ») est une maladie dégénérative de cause inconnue, touchant l’ensemble des systèmes dopaminergiques, cholinergique, noradrénergique et sérotoninergique
Physiopathologie 1A : Dans l’atteinte dopaminergique, le processus atteint d’abord la voie nigro-striatale (triade parkinsonienne à partir de 50-60 % de neurones perdus), puis dépasse cette voie (signes axiaux, signes non-moteurs). Cette dégénérescence est liée à la présence de corps de Lewy (inclusions intraneuronales avec agrégats d’alpha-synucléine)
Epidémiologie 3 :
– La prévalence augmentent progressivement avec l’âge jusqu’à 80 ans, 50% > 75 ans
– l’incidence augmentent également jusqu’à 80 ans, 1,4% débute avant 40 ans 1donnée issu de la source 3 +++. Le CEN note : pic à 60 ans, 10% avant 40 ans– Sex-Ratio H/F = 3/2
– 1ere cause de syndrome parkinsonien, 2e maladie neurodégénérative (après la maladie d’Alzeihmer) et 2e cause de handicap moteur d’origine neurologique chez le sujet agé (après les AVC)
Etiologie : L’étiologie reste inconnue. Probablement multi-factorielle
– Age +++
– Cause génétique (récessives ou dominantes) retrouvées chez 15 % des patients
– Cause environnemental : exposition au métaux lourd, solvant organique, manganèse, pesticide 2le CEN note les pesticides dans les FdR mais le manganèse dans les DD (dg diff)
2) Diagnostic 2
Le diagnostic est réalisé au bout de plusieurs années et doit être reconsidéré tous les 6 à 12 mois !
En cas de suspicion de maladie de Parkinson, une consultation neurologique est indispensable !
| Clinique | Paraclinique |
|---|---|
| Triade parkinsonnienne typique, unilatérale ou asymétrique Absence de « drapeaux rouges » et de facteurs iatrogènes explicatifs Réponse au traitement dopaminergique |
Aucun |
A ) Clinique
Le diagnostic est suspecté devant une akinésie / hypokinésie / bradykinésie associée à un autre trouble moteur.
Il est confirmé cliniquement par une nette réduction des signes moteurs à l’introduction du traitement dopaminergique (sensibilité aux traitements pendant au min. 5 ans) 1A
FdR :
– âge ++
– ATCD familiaux
– exposition toxique : milieu rural ou industriel
Signes moteurs :
– Triade du syndrome parkinsonien unilatérale / asymétrique tout au long de la maladie : Tremblement de repos (absent dans 30% des cas 1A), rigidité plastique et akinésie3ralentissement à l’initiation du mouvement et/ou hypokinésie4diminution de l’amplitude d’un mouvement et/ou bradykinésie5ralentissement à l’exécution du mouvement.
– instabilité posturale (chez le sujet âgé)
– dystonie focalisé de la main (crampe de l’écrivain) ou du pied (varus équin ou extension du gros orteil) chez le patient < 40 ans
Signes non-moteurs pouvant être présent au diagnostic
– Psy : apathie, dépression, anxiété
– Douleurs pseudo-rhumatismales (raideur de membre, périarthrite scapulo-humérale ++ 1A)
– Hyposmie (atteinte du noyau du centre olfactif 1A)
– Trouble du sommeil paradoxal (« rêves animés » responsables d’actes auto- ou hétéro-agressifs)
– Constipation
– Amaigrissement, asthénie…
B ) Paraclinique
Le diagnostic de maladie de Parkinson est clinique. Aucun examen complémentaire n’est justifié en cas de tableau typique !
Scintigraphie cérébrale (DaTSCAN) : utile dans le cadre de tremblements mixtes d’attitude, d’action et de repos. Elle consiste à marquer les terminaisons dopaminergiques ; une dénervation présynaptique est observée en cas de tremblement du à la maladie de Parkinson, mais également dans d’autres syndromes parkinsoniens dégénératifs
IRM cérébrale : normale 0 . 6Pour le coup c’est pas bien précisé, mais il ne semble y avoir de lésions que dans d’autres causes de sd parkinsonnien.
Le diagnostic de certitude peut être établi post-mortem par histologie cérébrale
C ) Diagnostic différentiel 1A
Autres syndromes parkinsoniens :
– Maladie de Wilson : IRM et bilan cuivre systématique si < 40ans.
– Autres pathologies dégénératives responsables de syndromes parkinsoniens atypiques : présence de drapeaux rouges !
– Causes vasculaires, toxiques
– Absence de réponse prolongée au traitement dopaminergique
– Progression rapide avec chutes précoces
– Sd cérébelleux / atteinte pyramidale
– Troubles oculomoteurs
– Signes corticaux (apraxie, aphasie, troubles sensitifs)
– Atteinte précoce…
… Cognitive
… Pseudo-bulbaire (dysarthrie, dysphagie)
… Dysautonomique (incontinence urinaire, hypotension orthostatique sévère)
Autres mouvements anormaux, en particulier le tremblement essentiel 2
3) Evolution 1A
A) Histoire naturelle
4 phases typiques
Phase diagnostique (= phase de début2) : signe typique pré-traitement
Lune de miel (= phase d’état2) : bon contrôle sous traitement. L’efficacité des traitements dopaminergiques est généralement prolongée plus de 5 ans.
Phase des complications motrices (= phase avancée2) : apparaissent en moyenne après 4 à 5 ans.
L’âge jeune de déclaration de la maladie de Parkinson est un facteur d’apparition précoce des complications motrices
Phase du déclin moteur et cognitif (= phase tardive2) : Dans les formes évoluées, le patient oscille entre un état parkinsonien sévère et une symptomatologie parkinsonienne modérée mais compliquée de dyskinésies. La démence atteint 30 % des patients, jusqu’à 80 % après 15-20 ans d’évolution.
B) Complications
-
Complications motrices
Fluctuations d’efficacité
– Akinésie de fin de dose : réduction progressive de la durée d’action de la L-dopa (perte de capacité de stockage) jusqu’à atteindre la demi-vie de la molécule, 60-90 min
– Akinésie de nuit et du petit matin : crampes des mollets et des orteils, difficultés pour se tourner dans le lit
– Phénomène « on/off » : passages parfois brutaux d’un état non-parkinsonien (on) / à un état parkinsonien sévère (off)
Dyskinésies
– Dyskinésie de milieu ou de pic de dose : mouvements involontaires surtout à type de chorée des membres et du tronc
– Dyskinésies biphasiques : mouvements involontaires plutôt dystoniques des membres inférieurs, souvent douloureux, lors d’une fluctuation d’état (début ou fin de dose)
-
Complications de la phase de déclin 2
Signes moteurs axiaux
– Dysarthrie (précoce d’évolution lente) : baisse progressive de l’intensité de la voie, monotonie de la parole, altérations de la qualité vocale, puis perte de la précision articulatoire
– Dysphagie (souvent précoce) : bavage et stase salivaire, difficultés de mastication, fausse route
– Troubles de la marche : enrayement cinétique = freezing (pieds « collés au sol » à l’initiation de la marche) ; festination (emballement brutal et incontrôlable, risque de chute)
– Troubles de la posture 1A : triple flexion, flexion du tronc en avant (= camptocormie) et latéralement (= syndrome de Pise)
– Troubles de l’équilibre postural, chutes en arrière
Douleur d’allure rhumatologique (60% des patients). Plusieurs types :
– La douleur musculosquelettique : liée à l’hypertonie et l’hypokinésie (ex blocage d’épaule).
– La douleur dystonique.
– La douleur neuropathique radiculaire ou centrale.
– L’akathisie (sensation pénible d’agitation interne avec nécessité impérieuse de bouger).
Troubles neuropsy :
– dépression
– anxiété
– trouble psychotique avec hallucination, parfois délire
– démence (jusqu’à 40% à la fin de vie)
– trouble du sommeil : fragmentation, réduction, insomnie d’endormissement, somnolence diurne, trouble du sommeil paradoxal
– trouble du comportement voir addiction comportementale : TCA, jeu pathologique, achats compulsifs, hypersexualité…
Troubles dysautonomiques :
– Digestif : nausée, constipation,
– Urinaire : nycturie, incontinence, urgence mictionnelle
– Hypotension orthostatique
– Sexuel : dysfonction érectile, éjaculation précoce, baisse de la libido (parfois hypersexualité sous agoniste dopam.)
– Hypersudation
-
Complications du traitement dopaminergique
Paragraphe à développer avec §8 du guide HAS
Les complications ci-dessus peuvent être totalement ou en partie secondaire au médicament
Effets indésirables du L-dopa : nausées, vomissements, hypotension orthostatique sévère, hallucinations voire délire paranoïaque parfois annonciateur d’une évolution en démence
Effets indésirables du des agonistes dopaminergiques : idem + troubles du comportement (TCA, jeu pathologique, achats compulsifs, hypersexualité…), fréquent (15%) mais réversibles à la diminution / l’arrêt.
Syndrome malin des neuroleptiques 2 : en cas d’arrêt brutal d’un traitement. Associe altération de la conscience + rigidité musculaire généralisée + hyperthermie + dysautonomie.
Syndrome de dysregulation dopaminergique 2 : surconsommation compulsive de traitement dopaminergique, souvent associé à des troubles comportementaux
4) PEC 1A
A) Bilan initial
Paragraphe à développer avec guide HAS
– point critique du parcours des soins p.18
– bilan pré-thérapeutique éventuelle p.38
– recherche mutation génétique (p.73)
B) Traitement
Paragraphe à développer avec guide HAS
Le traitement initial est toujours à réaliser par un neurologue (aucune urgence à débuter un traitement) 2
-
Mesures générales
ALD 100 %
Kinésithérapie : gymnastique quotidienne, équilibre postural, transferts…
Orthophonie à ne pas proposer trop tardivement !
Associations de patients
-
Traitement initial des troubles moteurs : restauration de la transmission dopaminergique
Molécules disponibles
| Traitement |
Mécanisme | Particularités |
|---|---|---|
| L-dopa + inhibiteur périphérique de la DDC (dopa décarboxylase) | Précurseur de la dopamine, inhibiteur périph. toujours associé pour limiter les effets indésirables | Le plus efficace et le mieux toléré |
| Agonistes dopaminergiques (pramipéxole, ropinirole, rotigotine, piribédil) | Action directe sur les récepteurs dopaminergiques | Moins efficaces et moins bien tolérés que la L-dopa, mais retarde l’apparition des complications motrices Effets indésirables : risques comportementaux +++ |
| Inhibiteurs de la mono-amine oxydase (IMAO-B) | Inhibition du métabolisme de la dopamine | Action modérée |
Remarques
– la dompéridone (neuroleptique antiémétique0) est coprescrit systématiquement
– les anticholinergiques sont devenus quasi-obselètes, ils gardent une indication pour des sujets jeunes avec symptomatologie résistant au traitement dopaminergique bien conduit.
– médicaments déconseillés : neuroleptiques anti-émétiques et anti-psychotique (exception : clozapine), autres médicaments responsables d’un syndrome parkinsonien2
Stratégie thérapeutique
Avant 65-70 ans
– Agoniste dopaminergique ou IMAO-B en 1ère intention
– Si symptômes non-contrôlés : progression poso. de l’agoniste dopaminergique, puis association à la L-Dopa ou IMAO-B
Après 65-70 ans
– L-dopa d’emblée (monothérapie) ou IMAO-B
– Si symptômes non-contrôlés : progression poso. de la L-dopa ou association avec IMAO-B
-
Traitement des formes évoluées / des complications
Les signes de la phase de déclin sont peu ou pas sensibles au traitement dopaminergique.
Fluctuations motrices
– En cas de blocage sévère : injection d’apomorphine par stylo
– Fractionnement de la L-Dopa (rapprochement des prises)
– L-dopa + agoniste dopaminergique ou augmentation des doses d’agoniste
– L-dopa + ICOMT (prolonge l’action périphérique de la L-dopa)
– IMAO-B
Dyskinésies
– Réduction des doses de L-dopa et plus grand fractionnement sur la journée (si dyskinésie de milieu de dose)
– ± Amantadine
Fluctuations et dyskinésies résistant aux traitements
– Stimulation à haute fréquence du noyau sous-thalamique / du pallidum interne : Indiquée chez des patients de < 70 ans avec complications motrices sévères ou symptômes handicapants malgré un traitement bien conduit (sans trouble cognitif sévère)
– pompe d’apomorphine SC ou administration continue de L-dopa via une gastrostomie
Hallucinations, délire : suppression progressive des anti-parkinsoniens sauf la L-Dopa. Traitement par clozapine en cas de persistance (risque d’agranulocytose, surveillance NFS)
Autres signes non-moteurs : prise en charge essentiellement symptomatique0 (PEC bien détaillée dans la ref. 2)
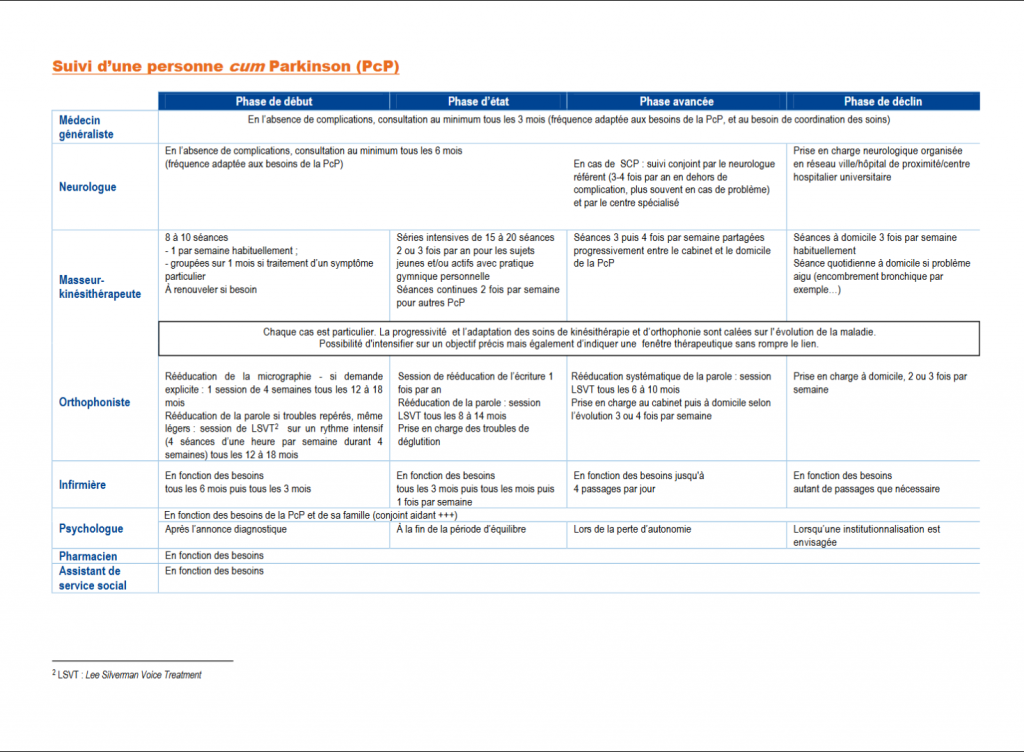
C) Suivi 2
Suivi multidisciplinaire
– Médecin généraliste : tous les 3 mois min.
– Neurologue : tous les 6 mois min.
– Kiné, orthophoniste, infirmier, psychologue, service social, pharmacien…
Objectif
– Recherche de signes moteurs évolutif
– Recherche de signes non-moteurs
– Identifier les troubles axiaux (posture, parole, déglutition) avec l’aide du kiné et orthophoniste
– Suivi du traitement médicamenteux





7 réponses à “Maladie de Parkinson”
Voir également la fiche mémo HAS 2016 : Maladie de Parkinson et syndromes apparentés : techniques et modalités de la prise en charge non médicamenteuse des troubles moteurs dont les messages clefs sont :
« – Aucune technique rééducative manuelle ou instrumentale n’a montré de supériorité par rapport aux autres.
– L’activité physique est une composante commune à toutes les techniques rééducatives ; elle permet également d’améliorer les capacités cognitives.
– Le mode de prise en charge et les moyens rééducatifs utilisés pour traiter les troubles moteurs et leurs conséquences doivent respecter les quatre principes suivants : l’intensité (au cours d’une période de prise en charge) ; la diversité ; la régularité ; la continuité (entre les périodes de prise en charge).
– Il est recommandé de proposer aux patients toute activité physique (marche, etc.) ou technique rééducative de son choix qui prend en compte ces quatre principes. »
Selon l’HAS, les neuroleptiques anti-émétiques sont déconseillés. Il n’est pas fait explicitement mention du domperidone, qui est un neuroleptique antiémétique … prescrit « systématiquement » selon le ref de neuro. Quid ?!
Domperidone est un antiémétiques périphérique car il ne traverse pas la barrière hemato encéphalique donc n’agit pas au niveau des récepteurs dopaminergique centraux c’est la raison pour laquelle il reste utilisé dans la maladie de Parkinson
Merci de votre commentaire, pourriez vous préciser vos sources ?
Selon le référentiel de Neuro CEN, le dompéridone n’est pas « systématiquement » prescrit mais seulement en cas de nausée et vomissements en limitant la prescription à une durée de ttt courte (7j max)
Concernant le traitement de derniers recours :
– chirurgie : implantation profonde d’électrode pour stimuler le noyau sous thalamique ou le pallidum interne
– administration continue d’APOMOMORPHINE SC
– pompe entérale de LEVO DOPA + CARBIDOPA (gastrotomie)
(source: DEBOECK NEURO CARDIO)
oui, la HAS en parle, la fiche est en cours d’amélioration. Merci !